Introducción
Las enfermedades de transmisión sexual (ETS), que con frecuencia se manifiestan como lesiones cutáneas genitales tanto en hombres como en mujeres, representan una causa habitual de consulta médica. Estas lesiones pueden corresponder a patologías benignas, premalignas, malignas o infecciosas, y suelen generar en los pacientes sentimientos de ansiedad, miedo y vergüenza, lo que en muchos casos retrasa o incluso impide la búsqueda de atención médica.
Dentro del diagnóstico diferencial de las lesiones cutáneas genitales, siempre deben considerarse las infecciones de transmisión sexual (ITS), así como las lesiones premalignas y malignas. No obstante, al analizar la etiología de estas lesiones, se observa que una gran proporción corresponde a condiciones benignas, en su mayoría de origen infeccioso o simples variaciones anatómicas sin implicancias patológicas.
Este capítulo tiene como objetivo proporcionar una guía práctica para médicos, tanto especialistas como no especialistas, que les permita abordar de manera adecuada el amplio espectro de lesiones genitales en el hombre relacionadas con ITS. Se busca facilitar un diagnóstico certero y un tratamiento oportuno, así como orientar sobre los criterios de derivación al especialista cuando sea necesario.
El abordaje inicial de un paciente con sospecha de ITS debe incluir una historia clínica detallada, con énfasis en los factores de riesgo: comportamiento sexual, antecedentes de exposiciones sexuales de riesgo, viajes recientes, patologías previas y hábitos de higiene. Es fundamental interrogar sobre síntomas como prurito, dolor, secreción o la presencia de otras alteraciones cutáneas.
Debe realizarse un examen físico minucioso de los genitales, describiendo cuidadosamente las características de la lesión: número (única o múltiple), color, consistencia, signos de inflamación o atrofia, presencia de secreción, adenopatías inguinales, entre otros.
En la mayoría de los casos, el diagnóstico puede establecerse con el examen clínico, siendo necesario recurrir a exámenes complementarios (laboratorio, microscopía o biopsia) sólo en una minoría de situaciones. Por ello, es fundamental que los profesionales de la salud estén capacitados para realizar un examen genital adecuado. Un diagnóstico precoz y preciso tiene importantes implicancias para el paciente y la salud pública:
- Permite tratar y prevenir la transmisión de ITS
- Facilita la detección de enfermedades sistémicas graves que requieren tratamiento
- Contribuye a evitar la progresión de lesiones premalignas
| Métodos de prevención de ITS |
|
Tamizaje en pacientes asintomáticos:
| Mujeres | Hombres |
|
Tamizaje recomendado para VIH |
En pacientes asintomáticos con exposición reciente a ITS:
- Examen físico: evaluación de genitales, región perineal y anal, región inguinal, y búsqueda de secreción uretral.
- Test rápido de VIH: si es negativo, repetir entre los 3 y 6 meses posteriores a la exposición.
- Serologías: anti-VHC, anti-HBs, HBsAg.
- Pruebas para sífilis (RPR o VDRL): en el momento de la consulta y a los 3 meses post exposición.
- HSV I y II: IgG e IgM, al menos una semana después de la exposición.
- Gonorrea y clamidia: test en secreción uretral o muestra de primera micción.
El enfoque actual para el manejo de ITS es predominantemente sindromático, más que etiológico. En la mayoría de los casos, se indica iniciar tratamiento empírico antes de contar con los resultados definitivos de laboratorio.
Úlceras genitales
Existen ulceras genitales de causa distinta a una ITS como, por ejemplo: infección bacteriana de piel, balanitis candidiásica complicada, Síndrome de Reiter, reacción fija a medicamento, Enfermedad de Behcet.
Con respecto a las ITS, las más frecuentes son por herpes genital, linfogranuloma venéreo, chancroide, granuloma inguinal y sífilis.
Herpes genital
El herpes genital es una infección viral crónica y de por vida. Corresponde a la causa más común de úlcera genital, cuyo agente etiológico es el virus herpes simplex (VHS).
Presenta dos variantes, el VHS-1, que tiende a causar más frecuentemente afecciones bucofaríngeas (herpes labial) y el VHS-2 que se encuentra más frecuentemente en afecciones genitales (herpes genital), además de ser más recurrente. Sin embargo, las prácticas sexuales han hecho que VHS-1 oral provoque herpes genital y el VHS-2 provoque lesiones bucales también.
La mayoría de las personas infectadas con VHS-2 no han sido diagnosticadas; muchas presentan infecciones leves o no diagnosticadas, pero excretan el virus de forma intermitente en la zona anogenital. En consecuencia, la mayoría de las infecciones por herpes genital se transmiten por personas que desconocen su infección o que son asintomáticas al momento de la transmisión.
El herpes genital se transmite por contacto genital, oro-genital u oro-anal. El virus penetra a través de microabrasiones o soluciones de continuidad de la piel o mucosas, para finalmente localizarse en las neuronas. Su período de incubación varía de 2 a 20 días con un promedio de 7 días. El cuadro clínico se presenta como primoinfección, latencia y recurrencias.
Primoinfección: La infección primaria por el VHS suele ser asintomática. En los casos sintomáticos el cuadro clínico se inicia con un pródromo caracterizado por prurito y ardor, asociado a una placa eritematosa localizada. Posteriormente aparecen vesículas en número variable de 1 a 3 mm de diámetro. Puede presentarse con fiebre, decaimiento, linfadenopatía regional y disuria. Las vesículas, generalmente múltiples, se ubican en el glande, prepucio o cuerpo del pene. La ruptura de estas vesículas provoca la formación de erosiones superficiales dolorosas. Las lesiones se resuelven entre 10 a 14 días. Puede haber lesiones en el ano y la zona perianal. La excreción viral puede persistir por tres semanas.
Recurrencias: Las recurrencias se presentan en más de un 80% de los pacientes. Éstas tienen una evolución clínica más atenuada y un período de excreción viral más corto, además de tener un pródromo. Algunas recurrencias pueden ser asintomáticas, pero con eliminación de partículas virales que pueden transmitir la enfermedad. La recurrencia puede desencadenarse por estrés físico y emocional, alteraciones del ciclo sueño-vigilia, relaciones sexuales, inicio del ciclo menstrual y fiebre mantenida. Los episodios recurrentes pueden prolongarse por sobreinfección bacteriana de las lesiones y por inmunodepresión
El diagnóstico clínico de la infección genital por VHS tiene una baja sensibilidad y especificidad, por lo que la confirmación de laboratorio de la infección y tipificación de VHS es esencial.
Se deben tomar muestras de la base de la lesión o de líquido de una vesícula. Dentro de las pruebas de diagnóstico se cuenta con:
– Test de Tzanck: Es un examen de citodiagnóstico donde se visualizan células gigantes multinucleadas típicas. Tiene baja especificidad y sensibilidad, por lo tanto, no debe confiarse en ella
– Serología: Los anticuerpos IgM se evidencian en suero 4 a 7 días después de la infección y alcanzan un máximo en 2 a 4 semanas. Las IgG aparecen luego de 1-3 meses y persisten durante toda la vida, por lo que resultan útiles sólo cuando se tiene antecedente evidenciado de seronegatividad o se registra aumento de títulos en dos muestras con 15 días de diferencia.
– PCR: Si bien la PCR ha sido el estándar diagnóstico para las infecciones por VHS del sistema nervioso central, hasta ahora el cultivo viral ha sido la prueba de elección para la infección genital por VHS. Sin embargo, la PCR para VHS, con su tasa de detección consistente y sustancialmente mayor, probablemente reemplazará al cultivo viral como el estándar de oro para el diagnóstico del herpes genital en personas con lesiones mucocutáneas activas, independientemente de la localización anatómica o el tipo viral. Su costo ha ido disminuyendo con el tiempo y hoy día es cada vez más accesible.
– Cultivo viral: Es actualmente el método gold standard para el diagnóstico de certeza. Sus inconvenientes son el costo y la demora en la obtención del resultado.
El tratamiento del herpes genital dependerá del estadío clínico en el que se presente. El objetivo del tratamiento es reducir la sintomatología, ya que no lo erradica ni tampoco previene recurrencia.
Primoinfección: se debe utilizar tratamiento farmacológico por vía oral. El tratamiento tópico no ha demostrado buena efectividad clínica. El tratamiento debe ser indicado precozmente para reducir la formación de nuevas vesículas, la duración del dolor, el tiempo de cicatrización y la excreción viral, pero no previene las recurrencias de la enfermedad. Se inicia con **Aciclovir 400 mg vía oral c/8 hrs por 7-10 días** o **Valaciclovir 1 gramo vía oral cada 12 hrs por 7-10 días**.
Recurrencias: Existen múltiples esquemas, pero el más frecuentemente utilizado es **Aciclovir 400 mg vía oral c/8 hrs por 5 días** o **Valaciclovir 500 mg vía oral cada 12 hrs por 3 días**.
Recidivante: Se aplica terapia de supresión cuando se producen más de 6 brotes de herpes genital dentro de un año, logrando una eficiencia de 60-70%. Se inicia **Aciclovir 400 mg vía oral c/12 hrs por 8-12 meses** o **Valaciclovir 1 gramo vía oral cada 24 hrs por 8-12 meses**. En caso de recurrencias durante la terapia de supresión, debe suspenderse ésta y tratar como un cuadro agudo, luego debe reiniciarse la terapia de supresión.
El tratamiento a la pareja sexual se realiza sólo si hay sintomatología, y de todos modos se le debe ofrecer estudio serológico.
No hay evidencia suficiente sobre seguridad y eficacia de aciclovir y valaciclovir en embarazadas.
Linfogranuloma venéreo
El linfogranuloma venéreo se ha descrito tradicionalmente como una enfermedad ulcerosa genital causada por las biovariedades L1, L2 y L3 de Chlamydia trachomatis, con un período de incubación de 3-30 días.
Es propia de países tropicales y subtropicales en África, Asia, centro y Sudamérica, pero que en los últimos 5 años ha presentando un resurgimiento en Europa y Norteamérica.
Se ha descrito una mayor asociación a hombres homosexuales y a pacientes con Virus de Inmunodeficiencia Humana (VIH) (inserte número de cita).
El linfogranuloma venéreo es a menudo asintomático, pero puede presentarse en tres estadios:
- Estadio primario: se observa una pápula o pústula indolora que evoluciona a úlcera, generalmente localizada a nivel balanoprepucial, vaginal, vulvar o cervical. Esta úlcera tiende a curar de forma espontánea en aproximadamente 7 días.
- Estadio secundario: aparece entre 2 y 6 semanas después del inicio, caracterizado por linfadenopatía inguinal o femoral dolorosa, unilateral, que puede ulcerarse, supurar o fistulizar.
- Estadio terciario: se presenta como un síndrome genito-ano-rectal, que incluye proctitis, fístulas, abscesos y en lesiones no tratadas que originan cicatrices y fibrosis pueden producir obstrucción linfática, generando elefantiasis de los genitales.
El diagnóstico de este cuadro es difícil por su escasa clínica y por falta de exámenes de certeza. Se basa en la sospecha clínica, la información epidemiológica, y la exclusión de otras causas de proctocolitis, linfadenopatía inguinal o úlceras genitales o rectales.
Como método complementario se puede recurrir a cultivo, a la Inmuno fluorescencia directa (IFD) o reacción en cadena de la polimerasa (PCR) cuando esté disponible, sobre muestras de fluido purulento aislado de ulcera, adenopatía o recto.
El tratamiento se basa en antibióticos sistémicos, donde el más utilizado es la **Doxiciclina en dosis de 100 mg vía oral c/12 hrs por 21 días**. En caso de alergia o intolerancia a Doxiciclina, se puede ofrecer esquema de:
- Eritromicina 500 mg vía oral c/6 hrs por 21 días (esquema utilizado en embarazadas).
- Azitromicina 1 gr vía oral al día por 21 días.
- Tetraciclina 500 mg vía oral c/6 hrs por 21 días
Se recomienda abstinencia sexual hasta pasados 7 días desde el inicio del tratamiento o hasta que se haya verificado la curación. Se debe tratar a toda pareja sexual de los casos en los últimos 30 días desde el inicio de la sintomatología.
Chancroide
También llamado chancro blando, corresponde a una infección bacteriana cuyo agente etiológico es haemophilus ducreyi.
Es poco frecuente en Chile, suelen presentarse casos en zonas portuarias por contacto sexual con personas procedentes de zonas tropicales donde esta patología es endémica. Su período de incubación es de 4 a 7 días.
La lesión característica de este cuadro es una pápula, única o múltiple, dolorosa con halo eritematoso que va evolucionando rápidamente a pústula y luego se forma una úlcera la cual no posee bordes irregulares, agudos y no indurada. Su base friable con tejido de granulación cubierta por un exudado y edema prepucial. En el hombre se localiza en el surco balano prepucial, frenillo, glande, prepucio y cuerpo del pene.
Para su diagnóstico, la clínica es crucial, y se deben utilizar los siguientes criterios:
- úlceras genitales dolorosas más adenopatías.
- no hay infección por treponema pallidum.
- no hay infección por virus herpes.
Como estudio complementario diagnóstico, se puede realizar cultivos (poco disponible) y PCR (no validada aún)
El tratamiento se basa en antibióticos sistémicos, con:
- Azitromicina 1 gr vía oral dosis única
- Ciprofloxacino 500 mg vía oral c/12 hrs x 3 días ó
- Ceftriaxona 250 mg vía intramuscular en dosis única o (esquema en embarazadas)
- Eritromicina 500 mg vía oral c/8 hrs por 7 días. (esquema en embarazadas)
Se debe reevaluar al paciente en 1 semana, ya que a los 3 días los síntomas remiten y la úlcera en 7 días se cura. Este proceso es más lento en lesiones de mayor volumen, en pacientes no circuncidados y en VIH (+)
Se debe tratar a toda pareja sexual de los casos en los últimos 10 días desde el inicio de la sintomatología
Granuloma inguinal
Infección bacteriana de tipo granulomatosa crónica de genitales y piel circundante. Su agente etiológico corresponde a klebsiella granulomatis. Tiene un período de incubación de aproximadamente 2-3 meses. Es endémica de algunas regiones tropicales y subtropicales.
Su lesión característica inicialmente es una pápula o nódulo firme que se abre formando una úlcera bien delimitada e indolora. Esta puede evolucionar hacia la curación o hacia la destrucción con extensión rápida, lenta o intermitente de una úlcera profunda, serpiginosa, con o sin lesiones epiteliales hipertróficas. Puede existir diseminación hematógena a hígado, bazo y huesos, aunque es poco frecuente. No presenta adenitis.
Para su diagnóstico es difícil obtener un cultivo de esta lesión, y el diagnóstico requiere la visualización en muestra de lesión cutánea bajo microscopia de los **cuerpos de Donovan**.
El tratamiento de elección es con **Azitromicina 1 gr. una vez por semana o 500 mg por día durante 21 días**. Como alternativa se administra también **Doxiciclina 100 mg, dos veces al día durante 21 días**, o **Ciprofloxacino 750 mg dos veces al día durante 21 días**, ó **Eritromicina 500 mg cuatro veces al día durante 21 días**.
Se debe tratar a toda pareja sexual de los casos en los últimos 60 días desde el inicio de la sintomatología
Sífilis
La sífilis es una enfermedad infectocontagiosa sistémica de evolución crónica, de origen bacteriano cuyo agente etiológico es el Treponema pallidum subespecie pallidum (Tpp), importante mencionar que existen otros subtipos de treponemas pallidum causantes de otras enfermedades que no causan sífilis (1).
El principal mecanismo de transmisión de Tpp es por vía sexual cuando hay lesión presente, sin embargo, también puede transmitirse vía transplacentaria, intraparto, transfusión sanguínea e inoculación accidental.
Según la Organización Mundial de la Salud (OMS), en 2022 se estimó que 8 millones de adultos de entre 15 y 49 años adquirieron sífilis, lo que representa una prevalencia global del 0,6% tanto en mujeres como en hombres.
En Chile gracias a los programas de prevención y tratamiento precoz la tasa de sífilis ha variado de 73,6 por 100.000 habitantes en 1980 hasta llegar a 19,7 por 100.000 habitantes el 2010 (2). Sin embargo, los últimos estudios han mostrado nuevamente un alza de la incidencia de sífilis tanto en hombres como mujeres en todos los rangos de edad, para el año 2020 la tasa es de 28,3 por 100.000 habitantes (3). Según datos oficiales del Ministerio de Salud de Chile (Minsal), la sífilis es la infección de transmisión sexual (ITS) más prevalente en el país. Entre 2017 y 2021, se notificaron un total de 70.660 casos de ITS, de los cuales aproximadamente el 50% correspondieron a sífilis, superando al VIH (30%) y a la gonorrea (15%).
El curso de la enfermedad, según los hallazgos clínicos, se ha dividido en una serie de etapas que se utilizan para ayudar a guiar el tratamiento y el seguimiento. Las formas precoces: **sífilis primaria, sífilis secundaria y sífilis latente precoz** corresponde a las formas que se presentan en el primer año luego del contagio en adultos y dos años en niños. Las formas tardías: **sífilis latente tardía y sífilis terciaria** corresponde a aquellas sífilis que se diagnostican posterior al año luego de la infección (o en las que se desconoce el tiempo de evolución).
Esta infección tiene un periodo de incubación de 3 a 90 días. En la fase primaria, la lesión esencial, conocida como **chancro sifilítico**, se caracteriza por aparecer en el punto de inoculación del treponema. Es una lesión característicamente indolora, con aspecto de pápula roja pequeña que se erosiona y evoluciona a una úlcera de fondo limpio e indurado y bordes solevantados. Puede ubicarse en cualquier parte del cuerpo donde haya ocurrido el contacto, pero en genitales masculinos es común en surco balano-prepucial, glande, o el cuerpo del pene; y puede estar asociada con adenopatía regional única o múltiple, indolora; en mujeres puede afectarse la vulva o pasar inadvertido, si compromete genitales internos. Sin tratamiento su remisión espontánea ocurre en 2-5 semanas (4).
Posterior a la fase primaria, sobrevienen periodos cíclicos asintomáticos (donde se clasifican a los pacientes como **sífilis latente precoz**) y formas secundarias. La **fase secundaria de la sífilis** corresponde a la diseminación hematógena del Tpp, suele aparecer 6 a 12 semanas posterior a una sífilis primaria y se manifiesta dentro de los 12 primeros meses después de la infección, cada brote tiene una duración habitualmente 6 a 8 semanas. Esta etapa corresponde a la más contagiosa por poseer alto recuento bacteriano y se caracteriza por gran variabilidad de lesiones en piel y/o mucosas. En piel puede verse un exantema asintomático de intensidad variable. En los genitales por ser áreas húmedas y calientes se desarrollan **condilomas planos (o condiloma latum)** y se presentan como pápulas o placas húmedas, redondeadas u ovaladas, de base ancha, de color eritematoso o grisáceo (en pacientes poco aseados es posible detectar un olor sui generis, descrito como ratón mojado). En las mucosas, se observan los **parches mucosos**, en forma de placas eritematosas o blanquecinas húmedas, en mucosa genital y bucal. Es característico de esta fase también lesiones papulares palmo-plantares conocidos como **clavos sifilíticos**, adenopatías generalizadas, sintomatología sistémica usualmente muy leve: fiebre, compromiso del estado general, mialgias, cefalea, etc. Este cuadro remite aproximadamente en 1-3 meses (5).
Existe la fase de **sífilis latente precoz**, que es aquella en donde el microorganismo está presente en el cuerpo, pero de forma asintomática. Puede durar años. Se clasifica en temprana si dura menos de 1 año, y tardía si dura más de 1 año. Sin tratamiento, previo a la existencia de antibióticos, aproximadamente un tercio desarrollaba sífilis terciara (5).
La **Sífilis terciaria** es aquella fase de la enfermedad, avanzada, donde existen manifestaciones clínicas sistémicas de mayor morbi-mortalidad afectando a distintos sistemas, tales como el sistema cardiovascular (endoarteritis aórtica), y aparición de **síndrome gomatoso (granulomas)** con compromiso en cualquier parte del cuerpo.
La **neurosífilis** puede presentarse asociada tanto a formas precoces como tardía y el cuadro clínico es variable, desde cuadros asintomáticos a cuadros sintomáticos como meningitis, formas meningo-vasculares y formas parenquimatosas como la tabes dorsal y la parálisis sifilítica. Se consideran subtipos de neurosifífilis el compromiso oftálmico y auditivo.
El diagnóstico de sífilis se realiza a través de antecedentes epidemiológicos, el examen físico y pruebas de serología no treponémicas (VDRL, RPR). Estas últimas en caso de resultar positivas, implica que debe confirmarse el diagnóstico mediante pruebas serológicas treponémicas (MHA-TP, FTA-ABS). Cabe destacar que las pruebas treponémicas permanecen positivas siempre, por lo que no tienen utilidad en el seguimiento de la enfermedad. Por lo anteriormente mencionado es que para el seguimiento y evaluación del tratamiento se utilicen las pruebas del VDRL y RPR (6).
A la semana de aparición del chancro, el 30% tiene serología positiva, mientras que a las 3 semanas el 90% es seropositivo. En la sífilis secundaria hay serología positiva en el 100%.
Existen falsos positivos: embarazo, enfermedades autoinmunes, enfermedades infectocontagiosas, dislipidemias, cáncer, vejez, uso de drogas ilícitas, uso de vacunas, entre otras.
Existen falsos negativos: Efecto Prozona (En sífilis con alta carga bacteriana, el reactivo no diluye bien y se bloquean los anticuerpos), Inmunodeprimidos, período de ventana de infección.
El manejo de la enfermedad lo constituye el uso de antibióticos sistémico, con el fin de prevenir sus graves complicaciones tales como la neurosífilis.
Dado que existe una “Norma de profilaxis, diagnóstico y tratamiento de las infecciones de transmisión sexual” y que es exigible por ley en Chile, debemos conocerla. Esta norma se encuentra disponible en:
http://www.repositoriodigital.minsal.cl/handle/2015/909
El tratamiento habitual, según esta norma, esta resumido en el siguiente cuadro:
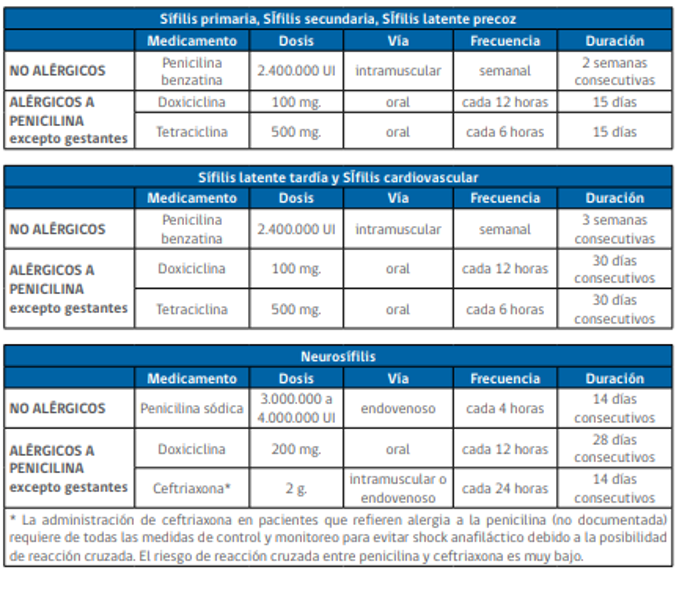
Para casos especiales como sífilis en pacientes VIH, gestantes, sífilis congénita, o sífilis en niños se revisar la norma antes señalada.
A la fecha de revisión de este texto (mayo del 2025), tenemos conocimiento que la nueva versión de esta norma, en Chile, se encuentra en proceso de revisión final, por lo cual se menciona que algunos aspectos señalados en este texto podrían cambiar.
Cabe mencionar, que en cada Servicio de Salud de Chile, se encuentran las UNACESS (Unidades de atención y control de Salud Sexual) donde se realiza diagnóstico y tratamiento de pacientes con ITS, excepto VIH. Estas unidades son gratuitas, independientes de la previsión de salud del paciente (FONASA, ISAPRE o personas sin seguro) y además son desectorizadas, por lo que se garantiza el acceso a las personas, independientes de su domicilio.
Referencias
- Giacani, L., & Lukehart, S. A. (2014). The Endemic Treponematoses. Clinical Microbiology Reviews, 27 (1), 89-115.
- Salvo A. Infecciones de transmisión sexual en Chile. [rev. med. clin. condes – 2011; 22(6) 813-824]
- Ministerio de Salud de Chile. (2021). Plan Nacional para la Prevención y Control del VIH/SIDA e ITS 2021–2022 (Resolución Exenta N.º 1111). Subsecretaría de Salud Pública. https://diprece.minsal.cl/wp-content/uploads/2022/03/RES.-EXENTA-N%C2%B0-1111-Plan-nacional-VIH-SIDA-e-ITS-2021-2022.pdf
- French P, Gomberg M, Janier M, Schmidt B, van Voorst Vader P, Young H: 2008 European guidelines on the management of syphilis. Int J Std Aids. 2009;20:300-9
- O’Farrell N. 2010 European guideline on donovanosis. IUSTI / WHO European STD guidelines. 2010.
- Scheinfeld N. Update on the treatment of genital warts. Dermatol Online J. 2013 Jun 15;19(6):18559.
Descarga Uretral (uretritis)/ Cervicitis
Las ITS supurativas por uretra son una variedad muy frecuente en nuestro medio y el mundo entero. En este grupo se incluye a aquellas patologías que generan salida de secreción uretral espontánea o posterior a la micción, acompañándose de forma variable con eritema alrededor del meato, disuria y en algunos casos, dolor testicular en hombres.
Cabe señalar que existen causas no infeccionas de similar sintomatología como lo son el edema post-instrumentación de vía urinaria, estenosis, síndrome de Reiter, litiasis uretral, etc.
Sin embargo, la mayoría de las veces, la causa es por una ITS de origen bacteriano. Dentro de ellas se encuentran aquellas por etiología gonocócica y aquellas no gonocócicas donde se incluye a chlamydia, ureaplasma y micoplasma spp (1).
En mujeres habitualmente el cuadro es menos sintomático que en hombres, y por ende de mayor tardanza en realizar e diagnóstico. La cervicitis es resultado de la inflamación del cérvix y los síntomas más frecuentes son: secreción endocervical purulenta o mucopurulenta visible en el canal endocervical o en muestra de hisopo endocervical.
Uretritis gonocócica
El agente etiológico es Neisseira gonorrhoeae, una bacteria diplococo gram (-), la cual tiene un período de incubación de 2-6 días. Está presente en el 10-20% de los casos de uretritis, y en nuestro país es una enfermedad de notificación obligatoria.
Frecuentemente existe coinfección con chlamydia trachomatis (2) y ureaplasma parvum/urealyticum.
El diagnóstico suele ser clínico, y a diferencia de la uretritis no gonocócica, aquí la mayoría son sintomáticos. Se presenta con sintomatología urinaria de almacenamiento y profusa secreción uretral purulenta. A largo plazo puede desarrollarse como consecuencia estenosis uretral. Otro cuadro menos frecuente es la epididimitis y más raramente la prostatitis.
En mujeres el cuadro mayoritariamente asintomático, y en algunos casos puede presentarse como uretritis, cervicitis, proceso inflamatorio pélvico.
En cuanto a los exámenes complementarios el **gold standart** es el cultivo de secreción uretral (cultivo de Thayer Martin o de agar-chocolate) para identificar el germen y estudiar su sensibilidad antibiótica.
Uretritis no gonocócica (UNG)
El organismo más frecuentemente aislado en las UNG, con un 15-40%, es el patógeno intracelular Chlamydia trachomatis serotipos D-K, con un período de incubación de 3-21 días.
Es frecuente que la uretritis por chlamydia coexista con uretritis gonocócica, por tanto, el tratamiento empírico debe incluir como ambos gérmenes (2). Otros gérmenes aislados, con similar sintomatología y período de incubación son en orden de frecuencia: mycoplasma genitalium (15-25%), ureaplasma parvum (3-11%). Gérmenes como ureaplasma urealyticum y mycoplasma hominis son menos frecuentes.
El diagnóstico es principalmente clínico, pese a que es frecuente que curse de forma asintomática. En hombres provoca clásicamente secreción uretral clara, ardor uretral y prurito uretral. Por otro lado, también puede presentarse como orquitis, epididimitis, o más raramente prostatitis.
Como exámenes complementarios debe realizarse cultivo de secreción uretral para lograr identificar germen y estudiar su sensibilidad. Es frecuente que no se logre identificar ningún germen en uretritis no gonocócica, siendo el más frecuente la chlamydia, seguido de micoplasma y ureaplasma, que por lo general son parte de la flora comensal, que pueden volverse patógenos en determinados momentos.
El cuadro en mujeres suele ser asintomático y en algunos casos: uretritis, cervicitis y proceso inflamatorio pélvico.
En los casos de sospecha de uretritis por ITS, se debe asumir que las uretritis gonocócicas y no gonocócicas habitualmente coexisten por tanto el tratamiento antibiótico debe contemplar cubrir ambos tipos de gérmenes (1).
Pacientes y sus parejas sexuales deben tener abstinencia sexual hasta que el tratamiento sea completo (para aquellos cuyo tratamiento sea la dosis única, la abstinencia debe ser de 7 días)
Los esquemas actuales en nuestra realidad local son:
- Ceftriaxona 500 mg. intramuscular + Azitromicina 1 gr. vía oral, ambos en dosis única.
- En alérgicos a la penicilina el tratamiento es con Doxiciclina 100 mg c/12 hrs x 7 días.
- Otros esquemas son Eritromicina 500 mg via oral cada 6 hrs x 7 días, o **Levofloxacino 500 mg via oral una dosis diaria x 7 días**.
- En embarazo no hay diferencias en el tratamiento
Se recomienda realizar seguimiento y control con cultivo a los 3 meses en aquellos pacientes en los que se sospechó gonorrea.
En los casos de las embarazadas debe realizarse control a los 3 meses con cultivo independientemente si contagió de gonorrea o chlamydias.
Con respecto a las parejas sexuales, todos deben ser evaluados por médico, y deben ser tratados todos aquellos que tuvieron relaciones sexuales 60 días previo al inicio de los síntomas. Si no ha tenido relaciones sexuales hace más de 60 días, se debe tratar a la última pareja sexual (1).
Referencias:
- Normas de manejo y tratamiento de enfermedades de transmisión sexual. Ministerio de Salud, Conasida, Santiago, 2016.
- Recomendaciones de expertos de la AEDV sobre el manejo de infecciones venéreas supurativas. Català y García-Hernández. ACTAS Dermo-Sifiliográficas 116 (2025) 68—80
- Salvo A. Infecciones de transmisión sexual en Chile. [rev. med. clin. condes – 2011; 22(6) 813-824]
- Centers for disease control and prevention. Sexually transmitted diseases treatment guidelines, 2021. Morbidity and Mortality Weekly Report.
Lesiones vegetativas
Condiloma acuminado (verruga genital)
Infección causada por algunos serotipos de virus papiloma humano (HPV). Es la enfermedad de transmisión sexual más frecuente, con más de 630 millones de infectados en el mundo. Los resultados muestran una prevalencia de 16 por 100 mujeres. A nivel nacional, datos del ISP reflejan que aproximadamente 16% de las mujeres se encuentran infectadas con VPH, en Santiago con una prevalencia de 14% en mujeres de 15 a 69 años. En hombres la tendencia apunta a un aumento en su incidencia, especialmente en hombres que tienen sexo con hombres (HSH) y personas que viven con VIH. En países que cuentan con programas de vacunación contra VPH, se ha documentado una reducción significativa de la incidencia de verrugas genitales en población joven vacunada.
Su periodo de incubación varía de 1 a 6 meses, y puede permanecer latente sin lesión por un período prolongado desde meses hasta años. El contagio se produce por contacto de piel sana con piel infectada en la relación sexual. No existe documentación de contagio por sangre o algún otro fluido corporal.
El VPH rara vez evoluciona a **cáncer cervicouterino, cáncer de pene, cáncer anal o tumor de Bushke-Lowenstein**.
La mayor parte (90%) de las verrugas genitales y anales son causadas por HPV tipos 6,11 a diferencia de las neoplasias malignas asociadas a HPV de tipo 16 y 18 que dan cuenta del 70% de cánceres cervicouterinos. Actualmente no existe evidencia de que las verrugas genitales evolucionen a cáncer cervicouterino.
La mayoría de las infecciones por HPV (90%) son asintomáticas, subclínicas o no detectables. Las lesiones son pápulas rosadas o de color piel, crecen como proliferaciones filiformes en su superficie que le dan un aspecto de **coliflor**. Pueden ser condilomas exofíticos cutáneos o mucosos, condilomas papulosos mucocutáneos, condilomas espiculados, planos ó maculares. Suelen ser pruriginosas, o menos común dolorosas o friables. Se desarrollan principalmente en superficies húmedas y su ubicación depende del lugar de inoculación y puede ser en el prepucio, glande, meato urinario y uretra.
El **diagnóstico es clínico**, y debe examinarse el área genital, meato urinario, pubis, región inguinal y región anal. Sin embargo, en determinadas situaciones se aconseja realizar biopsia:
- Diagnóstico dudoso.
- Lesiones que no responden o se agravan durante la terapia.
- En paciente inmunocomprometido.
- Si las lesiones son duras, hiperpigmentadas o ulceradas.
La histopatología muestra células escamosas con halo perinuclear. No existe mayor beneficio en identificar VPH, así como tampoco realizar PCR de VHP.
El objetivo del tratamiento es **eliminar verrugas sintomáticas**. Se debe tener claro que la eliminación de las verrugas genitales no implica la eliminación del VPH, ya que éste puede alojarse en piel sana, es por esto que el VPH es frecuentemente recurrente. Se pueden subdividir en aquellos realizados por el propio paciente o por el personal médico:
- **Acido tricloroacético al 80-90%** aplicado por especialista entrenado, a cada lesión y luego dejar secar, de forma semanal.
- **Tintura de Podofilino al 10-30%** en solución alcohólica, por médico o matrona entrenada, en cada lesión. Lavar zona aplicada con agua 1-4 horas después. Se puede aplicar de forma semanal. No utilizar más de 0.5 cc de solución o superficie mayor a 10 cm2. Contraindicado en embarazadas.
- **Crioterapia con nitrógeno líquido** solo por médico dermatólogo entrenado en su uso, cada 1-2 semanas según sea necesario.
- **Escisión quirúrgica** por “shaving” (afeitado), escisión tangencial con tijeras, curetaje y electrocoagulación.
- **Podofilotoxina al 0,5 a 1%** (gel tópico) para ser auto aplicado por paciente, con enseñanza del médico de la forma de aplicarlo. 2 veces al día por 3 días, descansar 4 días (4 ciclos)
- **Crema de Imiquimod crema al 5%** para ser auto aplicado por paciente en la noche 3 veces por semana, en días alternos, dejar por 6 a 10 hrs y lavar, por un período de hasta 16 semanas. No debe usarse en embarazadas. Tiene un éxito de clearence de verrugas del 50% a las 10 semanas. El tratamiento de cauterización con uso previo de Imiquimod tiene mejores resultados clínicos que la resección solamente.
En aquellas verrugas condilomatosas que aparecen en el meato urinario:
- Crioterapia o excisión
- Tintura de Podofilino al 10-30% en solución alcohólica, por médico o matrona entrenada, en cada lesión. De forma semanal, y siempre hay que dejar secarse.
En aquellas verrugas condilomatosas que aparecen intrauretrales:
- Excisión: a través de pinzas de biopsia fría mediante un cistoscopio, idealmente logrando cauterizar la base de la verruga para que no sangre.
- Fulguración con láser: Nd: YAG laser
- Instilación intrauretral con 5-FU: sirve como método de prevención de recurrencias una vez ya tratadas las verrugas. RAM: disuria, estenosis meatal, meatitis, irritación escrotal, úlceras uretrales. 1 vez a la semana por 6 semanas.
Luego del tratamiento se debe controlar con cistoscopia a los 3-6 meses
Todos los pacientes deben controlarse a los 3 meses del tratamiento, ya que en ese periodo es donde se presentan la mayor cantidad de recurrencias Las terapias en uso pueden reducir, pero no eliminar la infectividad, pudiendo recurrir en algunos casos.
No hay evidencia definitiva que un tratamiento sea superior a otros, o que un tratamiento sea más efectivo para todos los pacientes o todos los tipos de condiloma.
En la última década, la prevención de la infección por HPV se ha establecido gracias al desarrollo de vacunas altamente eficaces. La **vacuna bivalente (Cervarix®)**, que cubre serotipos 16 y 18, y la **tetravalente (Gardasil®)**, que cubre serotipos 6, 11, 16 y 18, han demostrado ser seguras, inmunogénicamente efectivas y eficaces en múltiples ensayos clínicos. Cervarix® fue aprobada por la FDA para mujeres no embarazadas entre 9 y 25 años, y Gardasil® para hombres y mujeres no embarazadas entre 9 y 26 años. Ambas vacunas han mostrado eficacia frente a la infección persistente por HPV y el desarrollo de lesiones intraepiteliales, mientras que Gardasil® también previene además las verrugas genitales.
Actualmente se dispone de la **vacuna nonavalente Gardasil 9®**, que amplía la cobertura a los serotipos 6, 11, 16, 18, 31, 33, 45, 52 y 58. En 2022, la Organización Mundial de la Salud (OMS) respaldó el uso de una sola dosis como esquema efectivo en adolescentes y adultos jóvenes sanos. En línea con esta recomendación, en 2025 Chile incorporó Gardasil 9® al Programa Nacional de Inmunizaciones (PNI) como esquema en **dosis única** para niños y niñas de 4º año básico. En personas inmunocomprometidas, se mantiene el esquema de 2 o 3 dosis, según edad y condición clínica.
Tradicionalmente, la vacunación consideraba tres dosis: al inicio, al mes y a los seis meses. El momento ideal para vacunar sigue siendo antes del inicio de la vida sexual. Aunque la vacuna no tiene efecto terapéutico una vez establecida la infección, es fundamental completar el esquema correspondiente para asegurar su efectividad. Cabe recordar que la vacunación no reemplaza el screening anual para cáncer cervicouterino
Parasitos
Las infecciones parasitarias del tracto genitourinario masculino son un tema de salud pública, aunque su incidencia varía considerablemente según la región geográfica y las prácticas de higiene y sexuales.
Tricomoniasis (Trichomonas vaginalis)
Es la infección de transmisión sexual (ITS) no vírica más común a nivel mundial. Se estima que en 2020 se produjeron 156 millones de nuevos casos de infección por T. vaginalis entre personas de 15 a 49 años, con una distribución equitativa entre hombres y mujeres (aproximadamente 82.6 millones en hombres). Los hombres suelen ser **portadores asintomáticos**, lo que contribuye a la propagación de la infección. La transmisión es principalmente por **contacto sexual directo**.
Aunque muchos hombres son asintomáticos, T. vaginalis puede causar **uretritis, epididimitis, prostatitis** y **alteraciones en la calidad del semen**. Los síntomas, si presentes, incluyen secreción uretral, disuria y prurito uretral. La ausencia de síntomas en hombres dificulta el diagnóstico y el tratamiento oportuno, lo que puede llevar a reinfecciones de sus parejas sexuales.
El tratamiento de elección son los antibióticos orales:
- Metronidazol (Flagyl): Puede administrarse en **megadosis (dosis única de 2 gramos)** o en **dosis múltiples (500 mg dos veces al día durante 7 días)**.
- Tinidazol (Tindamax): También se puede usar en **dosis única de 2 gramos**.
- Secnidazol (Solosec): Una **dosis única de 2 gramos**.
Consideraciones:
Es crucial que los pacientes completen el ciclo de tratamiento, incluso si los síntomas mejoran.
Se debe **evitar el consumo de alcohol** durante el tratamiento con metronidazol y hasta 3 días después de finalizarlo, debido a la posibilidad de una **reacción disulfirámica** (náuseas, vómitos, calambres, dolor de cabeza).
**Todas las parejas sexuales recientes deben ser evaluadas y tratadas simultáneamente** para prevenir la reinfección.
Se recomienda una nueva prueba entre 2 semanas y 3 meses después del tratamiento para confirmar la erradicación y descartar reinfección.
Escabiosis (Sarcoptes scabiei)
Es un problema de salud pública mundial, especialmente en países pobres y en vías de desarrollo.
Se transmite principalmente por **contacto directo piel con piel**, incluyendo el contacto sexual.
Es una **parasitosis familiar o de grupos cerrados**, con un alto porcentaje de contagios dentro de estos grupos. La prevalencia aumenta en otoño e invierno.
La sarna puede afectar el área genital, causando **prurito intenso**, **pápulas eritematosas** y **costras**. Las lesiones se localizan en el vello genital, pliegues inguinales y los genitales.
El tratamiento se basa en la aplicación de cremas o lociones específicas:
- Permetrina al 5%: Es el tratamiento de elección. Se aplica en todo el cuerpo, desde el cuello hacia abajo, y se deja actuar durante 8-14 horas antes de enjuagar. Puede ser necesario **repetir la aplicación una semana después**.
- Ivermectina oral: En casos de sarna severa o resistente, o en brotes epidémicos, se puede usar ivermectina oral, bajo supervisión médica.
Consideraciones:
Es esencial **tratar a todas las personas en contacto cercano** al mismo tiempo, incluso si son asintomáticas.
Se deben **lavar a máquina con agua caliente y secar a altas temperaturas** la ropa de cama, ropa y toallas utilizadas en los 3 días previos al tratamiento. Los artículos que no se puedan lavar deben sellarse en una bolsa de plástico durante al menos 72 horas.
El **prurito puede persistir** durante varias semanas después del tratamiento debido a una reacción alérgica a los ácaros muertos.
Pediculosis (Phthirus pubis) – Piojo púbico o «ladilla»
Es una **ectoparasitosis** específica del hombre, causada por Phthirus pubis (piojo del pubis). Es un insecto hematófago que se transmite principalmente por **contacto sexual o por fómites** (sábanas, toallas). Es prevalente en poblaciones sexualmente activas.
Las lesiones se ubican en el vello genital, pliegues inguinales y los genitales, causando **prurito intenso** y lesiones por rascado, así como la visualización de los **piojos o sus liendres** adheridas al vello.
Para su tratamiento, se utilizan lociones o cremas pediculicidas:
- Permetrina al 1% (loción o crema): Se aplica en la zona afectada y se deja actuar según las indicaciones del producto.
- Malatión (loción): Otra opción efectiva.
- Ivermectina oral: Puede considerarse en casos resistentes.
Consideraciones:
Puede ser necesario **afeitar el área afectada** en casos de infestación severa.
**Las parejas sexuales también deben ser examinadas y tratadas**.
La ropa, ropa de cama y toallas deben **lavarse con agua caliente y secarse a altas temperaturas**.
Esquistosomiasis (Schistosoma haematobium)
La **esquistosomiasis urogenital** es causada por Schistosoma haematobium y es **endémica** en algunas partes de África y Oriente Medio. Aunque es rara en muchos países, el aumento de la movilidad poblacional ha llevado a un incremento de casos importados. Afecta principalmente a comunidades pobres y rurales.
Los gusanos viven en los vasos sanguíneos alrededor de la vejiga y pueden liberar huevos en la orina. La infección puede causar **hematuria**, anemia, desnutrición, insuficiencia renal y, a largo plazo, **cáncer de vejiga**.
Tratamiento:
- Praziquantel: Es el fármaco de elección para todas las especies de Schistosoma. Se administra en **dosis única (40 mg/kg de peso)**.
Consideraciones:
El diagnóstico se realiza buscando **huevos del parásito en la orina** o mediante pruebas serológicas.
El tratamiento es fundamental para prevenir complicaciones a largo plazo.
Oxiuriasis (Enterobius vermicularis)
Comúnmente conocida como **»lombrices»**, es una **infección intestinal**, pero puede causar **prurito anal y genital** debido a la migración de las hembras grávidas para depositar sus huevos en la región perianal, especialmente por la noche. Es una **infección familiar** prevalente en colegios e internados.
Aunque es una infección intestinal, el prurito anal puede extenderse a la región genital, llevando a irritación y posibles infecciones secundarias por rascado.
El tratamiento de las parasitosis genitales masculinas depende del agente etiológico específico y la gravedad de la infección. Es fundamental **tratar simultáneamente a las parejas sexuales** para prevenir reinfecciones.
Tratamiento:
- Mebendazol: Dosis única de **100 mg, repetida a las 2 semanas**.
- Albendazol: Dosis única de **400 mg, repetida a las 2 semanas**.
- Pamoato de pirantel: Dosis única.
Consideraciones:
Es importante **tratar a todos los miembros de la familia convivientes**, ya que la infección es muy contagiosa.
Medidas de higiene como **lavarse las manos frecuentemente** (especialmente después de ir al baño y antes de comer), **cortarse las uñas** y **limpiar la ropa de cama regularmente** son cruciales para prevenir la reinfección.
Referencias:
- Organización Mundial de la Salud (OMS). Tricomoniasis. (Última actualización: Noviembre 2024). Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/trichomoniasis
- Mayo Clinic. Tricomoniasis – Diagnóstico y tratamiento. (Última actualización: Julio 2022). Disponible en: https://www.mayoclinic.org/es/diseases-conditions/trichomoniasis/diagnosis-treatment/drc-20378613
- MedlinePlus. Prueba de tricomoniasis. (Última actualización: Julio 2023). Disponible en: https://medlineplus.gov/spanish/pruebas-de-laboratorio/prueba-de-tricomoniasis/
- Cochrane. Fármacos para el tratamiento de la esquistosomiasis urinaria. (Última actualización: Agosto 2014). Disponible en: https://www.cochrane.org/es/CD000053/INFECTN_farmacos-para-el-tratamiento-de-la-esquistosomiasis-urinaria
- MSD Manuals. Uretritis. (Última actualización: Enero 2025). Disponible en: https://www.msdmanuals.com/es/hogar/trastornos-renales-y-del-tracto-urinario/infecciones-urinarias-iu/uretritis
- Apt, W. (2014). Infecciones por parásitos más frecuentes y su manejo. Revista Médica Clínica Las Condes, 25(3), 527-537. Disponible en: https://www.clinicalascondes.cl/Dev_CLC/media/Imagenes/PDF%20revista%20m%C3%A9dica/2014/3%20abril/12-Dr.Apt.pdf
- SEIMC. Diagnóstico microbiológico de las infecciones de transmisión sexual y otras infecciones genitales. Disponible en: https://seimc.org/contenidos/documentoscientificos/procedimientosmicrobiologia/seimc-procedimientomicrobiologia24a.pdf
- Elsevier. Tratamiento de las enfermedades causadas por parásitos. Disponible en: https://www.elsevier.es/es-revista-enfermedades-infecciosas-microbiologia-clinica-28-articulo-tratamiento-las-enfermedades-causadas-por-S0213005X09005059
Moluscum Contagioso
El Molusco Contagioso (MC) es una **infección viral cutánea común**, causada por un poxvirus (Molluscipoxvirus), virus ADN de la familia Poxviridae.
Si bien puede afectar cualquier parte del cuerpo, en adultos, especialmente en hombres, las **lesiones genitales son frecuentes** y a menudo se consideran una **infección de transmisión sexual (ITS)**.
La transmisión principal ocurre por **contacto directo piel con piel**. En adultos, esto incluye frecuentemente el contacto sexual. También puede propagarse por autoinoculación (rascarse o tocar las lesiones y luego tocar otras partes del cuerpo) y por fómites (objetos inanimados contaminados como toallas, ropa, equipos deportivos o de baño). Se han reportado casos de diseminación a través de la electrólisis y tatuajes.
Aunque es más común en niños (con picos de incidencia entre los 2-3 años y 10-12 años, a menudo asociado a piscinas), en adultos sexualmente activos, el molusco contagioso genital es una ITS.
La incidencia máxima en adultos sexualmente activos se sitúa entre los 16 y 25 años de edad.
En hombres, las lesiones suelen aparecer en los **genitales (pene, escroto, pubis), la cara interna de los muslos y la parte inferior del abdomen**. En hombres jóvenes inmunosuprimidos, las lesiones en la cara son frecuentes y pueden diseminarse al afeitarse.
Las personas con un **sistema inmunitario debilitado**, como aquellos con **VIH/SIDA**, trasplantados, o bajo tratamientos inmunosupresores, tienen un riesgo significativamente mayor de desarrollar molusco contagioso. En estos pacientes, las lesiones pueden ser **más numerosas, extensas, de mayor tamaño, persistentes y refractarias** a los tratamientos habituales. La prevalencia en pacientes con VIH puede ser del 10% al 20%, y las lesiones pueden ser atípicas, con tendencia a confluir y formar placas.
El **período de incubación** promedio es de **2 a 7 semanas**, aunque puede oscilar entre 15 días y varios meses (incluso hasta 7 meses).
En individuos inmunocompetentes, el molusco contagioso es generalmente una **infección autolimitada**, lo que significa que las lesiones suelen desaparecer por sí solas sin tratamiento en un período de **6 meses a 2 años**. Sin embargo, pueden persistir por períodos más largos (hasta 5 años) en personas inmunocomprometidas.
Las lesiones son **pápulas firmes, perladas o rosadas, con una característica umbilicación central** (una depresión en el centro). Su tamaño varía de **1 a 5 mm**, aunque en inmunodeprimidos pueden ser más grandes (hasta 20 mm). Generalmente **no son dolorosas**, pero pueden causar **prurito (picazón) ocasional**, lo que puede llevar a la autoinoculación y diseminación de las lesiones.
Aunque el molusco contagioso es autolimitado en personas sanas, el tratamiento a menudo se recomienda en el área genital para:
- Prevenir la autoinoculación y la diseminación de las lesiones a otras partes del cuerpo.
- Reducir el riesgo de transmisión sexual a las parejas.
- Por motivos estéticos o para aliviar el prurito o la incomodidad.
- En pacientes inmunocomprometidos, donde las lesiones pueden ser más persistentes y extensas.
El tratamiento puede ser realizado por un médico o, en algunos casos, aplicado por el propio paciente, buscando la opción más conveniente, tolerada y efectiva.
Tratamientos Físicos (Realizados por un profesional de la salud):
- Curetaje: Es el raspado de las lesiones con una pequeña herramienta quirúrgica llamada cureta. Es rápido y efectivo, pero puede requerir anestesia local y dejar pequeñas cicatrices o cambios en la pigmentación.
- Crioterapia: Congelación de las lesiones con nitrógeno líquido. Es un método rápido y efectivo, pero puede causar ampollas, dolor y ligera decoloración de la piel. Pueden ser necesarias varias sesiones.
- Láser: La terapia con láser (por ejemplo, láser de CO2) puede ser una opción para eliminar las lesiones de forma precisa, especialmente en zonas sensibles o en casos de lesiones numerosas o resistentes, y suele tener un bajo riesgo de cicatrices.
- Electrocauterización: Destrucción de las lesiones mediante calor generado por corriente eléctrica.
Tratamientos Tópicos (Medicamentos aplicados sobre la piel):
- Cantaridina: Es un agente vesicante que provoca ampollas y desprendimiento de las lesiones. Es un tratamiento que debe ser aplicado por un profesional de la salud y bajo supervisión.
- Podofilotoxina (en crema o solución): Destruye las células infectadas por el virus. Es un tratamiento que el paciente puede aplicar en casa bajo la supervisión de un médico.
- Imiquimod en crema: Este medicamento estimula la respuesta inmunológica local para combatir el virus. Puede ser efectivo, aunque su mecanismo de acción es indirecto y puede tardar más en mostrar resultados.
- Ácido Salicílico o Ácido Tricloroacético: Ayudan a exfoliar la piel y a la eliminación de las lesiones.
- Hidróxido de potasio (5-10%): Se utiliza para inducir una irritación local que lleva a la eliminación de las lesiones.
Consideraciones Adicionales:
En pacientes inmunocomprometidos (especialmente con VIH): Además de los tratamientos locales, el **tratamiento antirretroviral (TARV)** es fundamental. Al mejorar el sistema inmunitario, las lesiones de molusco contagioso pueden reducirse o desaparecer, aunque en algunos casos pueden ser más resistentes y requerir un manejo más intensivo.
Higiene y Prevención:
- **Evitar el contacto directo con las lesiones.**
- **No rascarse** ni frotar las lesiones, ya que esto puede diseminar el virus (autoinoculación).
- **Evitar compartir objetos personales** como toallas, ropa, cepillos.
- Mantener una **buena higiene corporal** y lavarse las manos con frecuencia.
- **Evitar el contacto sexual** mientras haya lesiones visibles en el área genital para prevenir la transmisión a la pareja. Los condones pueden ayudar a reducir la propagación, pero no previenen completamente la transmisión si las lesiones están en áreas no cubiertas por el condón.
- Cubrir las lesiones con ropa o apósitos para reducir el riesgo de transmisión.
El molusco contagioso puede reaparecer, ya sea por autoinoculación, reinfección o nuevas lesiones que emergen de la incubación.
Referencias:
- Mayo Clinic. (2024). Molusco contagioso – Síntomas y causas. Recuperado de https://www.mayoclinic.org/es/diseases-conditions/molluscum-contagiosum/symptoms-causes/syc-20375226
- Mayo Clinic. (2024). Molusco contagioso – Diagnóstico y tratamiento. Recuperado de https://www.mayoclinic.org/es/diseases-conditions/molluscum-contagiosum/diagnosis-treatment/drc-20375230
- MSD Manuals. (s.f.). Molusco contagioso – Trastornos dermatológicos. Recuperado de https://www.msdmanuals.com/es/professional/trastornos-dermatol%C3%B3gicos/enfermedades-cut%C3%A1neas-virales/molusco-contagioso
- MedlinePlus. (2021). Molusco contagioso. Recuperado de https://medlineplus.gov/spanish/ency/article/000826.htm
- Larralde, M., & Angles, V. (s.f.). Actualizaciones sobre Molusco contagioso. Sociedad Argentina de Pediatría. Recuperado de https://sap.org.ar/docs/publicaciones/fotoproteccion.pdf
- Monteagudo Sánchez, B. (s.f.). El molusco contagioso como infección de transmisión sexual. AGAMFEC. Recuperado de https://www.agamfec.com/pdf/CADERNOS/VOL16/n2/PDF%20WEB%20CAD%2016%20N2/11_Cartas_ao_director.pdf
- Roman, R. (2011). MOLUSCO CONTAGIOSO. Revisión y opciones de tratamiento. Medigraphic. Recuperado de https://www.medigraphic.com/pdfs/archivostgi/tgi-2011/tgi115g.pdf
- Clínica Merced. (s.f.). Molusco Contagioso. Especializados en Piel. Médicos Dermatólogos. Recuperado de https://clinicamerced.cl/dermatologia/molusco-contagioso/
VIH-HEPATITIS
Las infecciones de transmisión sexual causadas por el **virus de inmunodeficiencia humana (VIH)** y el **virus hepatitis A-B-C** tienen un comportamiento (salvo VHA) de patología crónica, cuya principal sintomatología es más bien sistémica y multi-orgánica, con manifestaciones genitales escasas o inespecíficas. El diagnóstico se realiza a través de **test de serología**, descritos al inicio de este capítulo y su tratamiento y seguimiento, requiere ser estudiado en otro apartado.
Lesiones por Infecciones no ITS
Balanitis
La **balanitis** es la **inflamación del glande** del pene, que afecta aproximadamente entre el 3% y el 11% de los varones a lo largo de su vida. La **postitis** es la **inflamación del prepucio**. Cuando tanto el glande como el prepucio están inflamados, la afección se denomina **balanopostitis** y se presenta en aproximadamente el 6% de los varones no circuncidados. La balanopostitis solo se presenta en varones no circuncidados. [1] [2] Sin embargo, dado que la balanitis y la balanopostitis suelen presentarse juntas, los términos se usan indistintamente.
Las causas infecciosas de la balanitis incluyen ciertos hongos, como la levadura, y ciertas bacterias o virus, incluidos aquellos que causan infecciones de transmisión sexual (ITS), como la gonorrea.
La balanitis **no se considera una ITS**. La afección en sí no es contagiosa, pero los microorganismos que la causan sí lo son. Los **episodios recurrentes** de balanopostitis deben alertar sobre la posibilidad de **diabetes oculta**, por lo que los pacientes con episodios recurrentes deben someterse a una prueba de glucosa en sangre.
La morbilidad de la balanitis se debe a las molestias prolongadas que sufre el paciente si no se trata, a los síntomas derivados de complicaciones como la **fimosis** y al diagnóstico tardío de una ITS, **neoplasia intraepitelial de pene** o **cáncer de pene**.
La **causa más común de balanitis es la higiene personal deficiente o inadecuada en varones no circuncidados**, lo que provoca una **infección por Candida**.
El ambiente cálido y húmedo bajo el prepucio del pene no circuncidado, la falta de aireación, el secuestro de orina y secreción o filtración uretral, y la acumulación de **esmegma** irritante promueven el crecimiento de organismos, más comúnmente Candida, que causan balanitis, lo que lleva a **eritema, irritación, edema, inflamación y molestias** en el glande del pene. [3] Las infecciones por hongos, particularmente aquellas causadas por Candida albicans, son las causas infecciosas identificables más comunes de balanitis y balanopostitis. [4] C. albicans normalmente está presente en la piel del glande y puede considerarse parte de la flora normal. Sin embargo, la colonización puede progresar a una infección directa bajo ciertas condiciones, particularmente en individuos con condiciones médicas subyacentes; mala higiene; hombres no circuncidados, especialmente aquellos con fimosis; o cambios en el pH basal. El riesgo de infección también es mayor en hombres cuyas parejas sexuales tienen infecciones vaginales recurrentes por Candida. [5] [6] La **diabetes** es el trastorno contribuyente subyacente identificado con mayor frecuencia. [3] [7]
Los hombres circuncidados tienen una prevalencia sustancialmente menor de balanitis (68%) en comparación con los hombres no circuncidados y que la balanitis se asocia con un **aumento de 3,8 veces en el riesgo de cáncer de pene**. [8] [9] Hasta el 45% de los pacientes con cáncer de pene informan antecedentes de balanitis. [10] [11] [12] [13]. Aunque las 2 entidades comparten algunos factores de riesgo comunes, como la presencia de un prepucio y la mala higiene genital, estos datos sugieren que la inflamación o infección crónica (balanitis) es un factor etiológico para el carcinoma de pene. [10] [11] [12] [13]
Aunque la infección por levaduras es la causa más comúnmente identificada de balanitis, se deben considerar muchas otras causas potenciales, incluidos agentes infecciosos y no infecciosos: [14] [15] [16]
Las etiologías infecciosas de la balanitis incluyen:
Bacterias anaeróbicas y aeróbicas como Bacteroides, Streptococcus y Staphylococcus, Borrelia vincentii y Borrelia burgdorferi, especies de Candida (más comúnmente asociadas con la diabetes), Chlamydia, Gardnerella vaginalis, Estreptococos betahemolíticos del grupo B y del grupo A, Virus del herpes humano 1 y 2, Virus del papiloma humano, Neisseria gonorrhoeae, Sarna, Treponema pallidum, Especies de Trichomonas.
Las etiologías no infecciosas de la balanitis incluyen:
Reacciones alérgicas al látex del condón y al gel anticonceptivo, autodigestión por enzimas exocrinas del trasplante pancreático activadas, Irritantes químicos, como espermicidas, detergentes, jabones perfumados y geles de ducha, suavizantes de telas y vaselina, Alergias a medicamentos, como tetraciclina, sulfonamida, fenacetina, espermicidas y lubricantes personales, Eccema, Afecciones edematosas, que incluyen insuficiencia cardíaca, cirrosis, anasarca y síndrome nefrótico, obesidad mórbida, Condiciones neoplásicas, Neoplasia intraepitelial del pene, Infiltración de células plasmáticas (balanitis de Zoon), Lavado excesivo, Mala higiene personal (lo más común), Trauma. Uso de fármacos glucosúricos en la diabetes (como canagliflozina, dapagliflozina y empagliflozina) [20].
La balanitis puede presentarse a cualquier edad y afecta aproximadamente a 1 de cada 25 niños y a 1 de cada 30 hombres no circuncidados a lo largo de su vida. Los **niños menores de 4 años** y los **hombres no circuncidados** constituyen los grupos de mayor riesgo. La balanitis afecta aproximadamente al **11 % de todos los pacientes varones** tratados por urólogos en Estados Unidos. A nivel mundial, aproximadamente el **3 % de los hombres no circuncidados** se ven afectados.
La balanitis es más probable si hay **fimosis**. Cuando los niños alcanzan aproximadamente los 5 años, el prepucio se retrae con facilidad y el riesgo de balanitis disminuye.
La **diabetes** es la afección subyacente más común que predispone a la balanitis en los hombres adultos. [7] En general, la balanitis afecta a aproximadamente el **16 % de los hombres con diabetes**, en comparación con tan solo el 5,8 % de los hombres sin diabetes. [18]
Existe una asociación entre la balanopostitis inespecífica y un pene no circuncidado, especialmente con fimosis. Los datos sugieren firmemente que la **circuncisión previene o protege** contra las dermatosis peneanas infecciosas comunes, aunque podría no existir una causalidad directa. [10] [19]
La balanitis es más común en hombres no circuncidados debido a la mala higiene y a la acumulación de **esmegma** debajo del prepucio. El esmegma es una sustancia blanquecina, espesa y blanda, compuesta de células cutáneas desprendidas, sudor y aceites sebáceos (sebo), que suele acumularse debajo del prepucio en hombres no circuncidados. Aunque el esmegma tiene un olor desagradable, suele ser inofensivo si se limpia regularmente del glande; sin embargo, puede infectarse en casos de balanitis.
En condiciones normales, el esmegma ayuda a lubricar el movimiento del prepucio; sin él, se producen traumatismos localizados por fricción e irritación. Aunque antes se creía que el esmegma era un factor de riesgo para el carcinoma de pene, estudios recientes sugieren que es inofensivo y no representa una amenaza para el cáncer. [10] [21]
Los **síntomas típicos** de la balanitis incluyen **dolor, enrojecimiento y secreción maloliente subprepucial**. La afección presenta una presentación clínica más fulminante en pacientes diabéticos e inmunodeprimidos. [17] Si se permite que la balanitis progrese sin tratamiento, puede desarrollarse **edema localizado**. La combinación de inflamación y edema puede provocar que el prepucio se adhiera al glande y también puede progresar a **celulitis** y **adherencias peneanas**.
La mala higiene, un prepucio apretado y la acumulación de esmegma, que sirve de foco para la proliferación bacteriana y fúngica, pueden provocar irritación localizada, infección e inflamación del glande y el prepucio. Las **infecciones fúngicas** suelen ser las responsables, siendo la más común la causada por *C. albicans*.
En algunos casos, **afecciones dermatológicas** como la psoriasis, el liquen plano o el liquen escleroso; reacciones alérgicas; o, con menor probabilidad, afecciones premalignas, pueden ser responsables. La sospecha de una **neoplasia maligna** subyacente justifica una biopsia diagnóstica o escisional. Los hallazgos clínicos en la exploración física pueden indicar otras etiologías con implicaciones para el manejo.
La historia del paciente debe incluir una evaluación del **riesgo de una ITS** y cualquier condición dermatológica subyacente, como eccema o psoriasis, o enfermedades sistémicas, como artritis reactiva o diabetes.
Además de una inspección cuidadosa del glande y el prepucio, el examen físico también debe incluir una **evaluación del meato uretral** para detectar inflamación, decoloración, estenosis y secreción, y cualquier manifestación extragenital como erupción generalizada, úlceras orales, linfadenopatía inguinal, infecciones de la piel, edema y artritis.
El uso de agentes diabéticos glucosúricos que aumentan la excreción urinaria de glucosa, incluidos canagliflozina (Invokana®), dapagliflozina (Farxiga®) y empagliflozina (Jardiance®), se ha relacionado con un **mayor riesgo de balanitis**. [22] [23] [24] [25]
Los síntomas suelen incluir **picazón, sensibilidad, ardor o molestias** en el glande. Puede presentarse dolor, prurito, irritación, edema, úlceras, disuria, llagas u otros signos de inflamación que afectan el glande y el prepucio. Estos síntomas suelen **empeorar después de las relaciones sexuales**.
Una exploración física que revela un **glande inflamado y eritematoso** confirma esencialmente el diagnóstico de balanitis. También pueden presentarse **pequeñas pápulas** con eritema irregular, **piel tirante** en el glande con **aspecto vidrioso o brillante**, y **manchas blanquecinas**. El glande puede ser **doloroso a la palpación** y el paciente puede experimentar **disfunción eréctil**, **incapacidad para retraer el prepucio** o dolor al hacerlo. Suele presentarse esmegma, que puede estar infectado. Puede haber linfadenopatía inguinal. Con menos frecuencia, la balanitis puede presentarse como una úlcera, simulando una ITS. Es improbable que se presenten síntomas sistémicos.
Ciertas características en el examen clínico, como el **exudado blanco cuajado** y la **secreción peneana**, hacen sospechar una **infección por Candida**. Se debe realizar un cultivo de cualquier secreción.
En los hombres no circuncidados, se debe evaluar la **movilidad y la firmeza del prepucio** para excluir complicaciones como la fimosis y la parafimosis.
La inflamación y el edema persistentes pueden causar **cicatrización y adherencia** del prepucio al glande. Con el tiempo, este proceso puede progresar a una **fimosis**
La balanitis también puede presentarse como una manifestación de **artritis reactiva o enfermedad de Reiter**. En estos casos, se manifiesta como **balanitis circinada**, a menudo asociada con inflamación articular, llagas en la boca y otros síntomas generalizados. [27]
La balanitis se diagnostica generalmente mediante **examen visual**, ya que la presentación clínica y el aspecto de las lesiones son suficientes. Sin embargo, puede ser necesaria una evaluación adicional según la historia clínica del paciente y los hallazgos físicos. Estas evaluaciones pueden incluir un cultivo bacteriano (por ejemplo, en presencia de exudado purulento), pruebas para el virus del herpes simple (VHS) (en presencia de lesiones vesiculares o ulcerativas), pruebas de sífilis (en presencia de una úlcera) y la detección de sarna, tricomonas y Mycoplasma genitalium (en presencia de uretritis).
La presencia de úlceras o vesículas peneanas **no descarta balanitis**, aunque estos hallazgos sugieren HSV o sífilis, respectivamente.
Por lo general, el **fracaso de un tratamiento estándar de balanitis durante 4 semanas** o el **crecimiento rápido** a pesar del tratamiento sugieren un diagnóstico de **carcinoma de pene**.
Para su tratamiento, se recomienda un **lavado genital adecuado** realizado suavemente con solución salina normal como terapia inicial para todos los pacientes con balanitis. [38]
Los **antimicóticos tópicos**, que suelen aplicarse dos veces al día durante 1 a 2 semanas o hasta que los síntomas se resuelvan, son el tratamiento de elección para la mayoría de los pacientes adultos con balanitis o balanopostitis. [39] Los **imidazoles tópicos**, como el **clotrimazol al 1%** y el **miconazol al 2%**, son las opciones preferidas de terapia de primera línea. [39] La **crema de nistatina** es una alternativa para pacientes alérgicos a los imidazoles. [39] El **ungüento de bacitracina** (no neosporina) generalmente se recomienda para niños con balanitis. [40]
En casos de **inflamación más grave**, la adición de **150 mg de fluconazol por vía oral** o la combinación de un imidazol tópico y un esteroide de baja potencia, como una **crema de hidrocortisona al 0,5 % o al 1 %**, aplicada dos veces al día, suele resolver el problema.
El tratamiento con un **antibiótico oral** (oxacilinas o cefalosporinas durante 7 días) y **crema tópica de mupirocina** aplicada 3 veces al día durante 7 a 14 días es adecuado si existe la sospecha de **celulitis concomitante o una infección secundaria**.
Las **infecciones anaeróbicas** se pueden tratar con **metronidazol**, mientras que las **infecciones aeróbicas** se pueden tratar con **cefalosporinas orales, eritromicina o amoxicilina/ácido clavulánico**. [39]
El **fracaso del tratamiento de primera línea** debe suscitar la preocupación de una posible infección secundaria o una **neoplasia maligna subyacente**. En tales casos, se deben obtener cultivos y considerar la realización de una **biopsia de tejido**.
Se recomienda la **circuncisión en casos recurrentes e intratables**, especialmente en pacientes inmunodeprimidos y diabéticos con fimosis significativa. En casos leves de fimosis que no sean demasiado graves, se puede considerar el uso de una **crema con esteroides** y una suave retracción manual del prepucio antes de recurrir a la intervención quirúrgica. [41] [42] [43]
En algunos casos, se puede intentar una dilatación suave de un prepucio estrecho con una pinza, pero esto puede dañar el glande y la uretra subyacentes, y está contraindicado si existen adherencias peneanas entre el glande y el prepucio. Este procedimiento suele requerir sedación o anestesia local.
En **situaciones de emergencia**, se puede realizar una **incisión (prepuciotomia) dorsal con anestesia local** para abrir un prepucio fimótico que interfiere con la micción y de otro modo impide un tratamiento efectivo. [44]
Mantener una **higiene adecuada**, como el lavado y secado frecuentes del prepucio, es una **medida preventiva esencial**. Sin embargo, el lavado genital excesivo con jabón o sustancias potencialmente irritantes puede agravar la afección. A las parejas sexuales femeninas de hombres con balanitis se les debe ofrecer la prueba de candidiasis o un tratamiento empírico para reducir el reservorio de la infección en la pareja. [28]
Existen varios tipos específicos de balanitis:
Balanitis por zoon: La balanitis circunscripta plasmacelular, también llamada balanitis por zoon, es una inflamación eritematosa del glande que también puede afectar el prepucio. Esta balanitis suele afectar a **hombres no circuncidados de mediana edad o mayores**, y se presenta como **placas eritematosas y brillantes, simétricas y bien delimitadas, con múltiples puntos rojizos, llamados manchas de pimienta de cayena**, en los tejidos afectados. El tratamiento generalmente consiste en la **circuncisión**.
Balanitis circinada: La balanitis circinada se asocia con la **artritis reactiva**, anteriormente conocida como enfermedad de Reiter. Esta balanitis se caracteriza por **úlceras pequeñas, superficiales, erosivas pero indoloras** en el glande. Puede presentarse como **placas eritematosas anulares con márgenes policíclicos** que afectan el meato. [45] Histológicamente, presenta pústulas en la epidermis superior de aspecto similar a la psoriasis pustulosa. También puede presentarse una dermatitis anular serpiginosa que a menudo presenta un aspecto **granular blanco grisáceo con un margen geográfico blanco**. [28] Esta lesión puede confundirse con psoriasis en la exploración física, e incluso la evaluación histológica no siempre permite distinguir con precisión entre ambos trastornos. [45]
La distinción entre balanitis circinada y psoriasis generalmente se realiza clínicamente con base en el historial de artritis reactiva o psoriasis. La **dermatoscopia** también puede ayudar a diferenciarla. [32] Si se sospecha clínicamente balanitis circinada en un paciente sin artritis reactiva conocida, se recomienda realizar pruebas de detección de ITS y del **antígeno leucocitario humano (HLA)-B27**. [45]
Balanitis queratósica y micácea pseudoepiteliomatosa: La balanitis queratósica y micácea pseudoepiteliomatosa es una **afección extremadamente rara** que se caracteriza por **lesiones cutáneas secas, escamosas, gruesas y verrugosas** en el glande, generalmente en **hombres circuncidados en edad avanzada**. [46] Aunque suelen ser benignas, estas afecciones pueden volverse localmente invasivas o progresar a **carcinoma verrugoso**. La etiología es incierta y el tratamiento varía según la gravedad de la presentación. [46] [47] El **5-fluorouracilo tópico** se puede utilizar en las etapas iniciales. [47]
Resumen del tratamiento
El **ungüento de bacitracina** se usa con mayor frecuencia en niños, mientras que el **clotrimazol o el miconazol** se suelen usar en adultos. Las **infecciones más graves** pueden requerir **fluconazol oral** y **crema de hidrocortisona**. Los **casos intratables** justifican una **biopsia** o una **circuncisión**. [17]
La gestión generalmente incluye lo siguiente:
- **Antifúngicos tópicos** para la balanitis inespecífica
- **Antimicóticos orales o sistémicos** para infecciones fúngicas graves o intratables
- **Antibióticos** (orales o tópicos) para infecciones bacterianas
- **Corticosteroides tópicos** para afecciones dermatológicas no infecciosas
- **Circuncisión** (o procedimiento de incisión dorsal) para fimosis significativa o sintomática
Si está disponible, considere la **dermatoscopia** en casos persistentes o intratables. Si el resultado es positivo o dudoso, proceda con una **biopsia, terapia ablativa o escisión**.
**Biopsia, ablación o escisión para lesiones premalignas y neoplásicas sospechosas**
Diagnóstico diferencial
Diversas afecciones cutáneas también pueden simular la balanitis. Algunos ejemplos son los siguientes: [39]
- La **dermatitis atópica** se presenta con **sequedad peneana, prurito, edema del glande y eritema**. Suele haber antecedentes de erupciones cutáneas inespecíficas recurrentes.
- La **dermatitis de contacto**, una afección inflamatoria de la piel, se produce por la exposición directa a irritantes o alérgenos. El tratamiento consiste en lavarse suavemente con agua y jabón y aplicar una **crema de hidrocortisona al 1 % dos veces al día**.
- El **eccema** es una afección cutánea crónica o prolongada que produce **picazón, enrojecimiento, agrietamiento y sequedad** en la piel. Se recomienda el tratamiento con **hidrocortisona al 1 % dos veces al día**. [39]
- El **liquen plano** es una patología cutánea que se caracteriza por **pequeñas manchas rosadas o moradas que pican**, generalmente en brazos o piernas y genitales masculinos. El tratamiento varía desde **esteroides tópicos moderados hasta ultrapotentes**, según la gravedad.
- El **liquen escleroso**, o **balanitis xerótica obliterante**, es un trastorno dermatológico autoinmune asociado con **decoloración blanquecina de la piel, hiperpigmentación, retracción cutánea y atrofia** que puede presentarse en el glande. Clínicamente, puede causar **estenosis y fimosis del meato urinario**, caracterizadas por una coloración blanca de la piel y constricción de la luz afectada. El tratamiento consiste en **esteroides tópicos ultrapotentes**, como el **propionato de clobetasol**, pero puede ser necesaria la cirugía, como la circuncisión, la incisión dorsal o la meatotomía.
- La **psoriasis** es una afección cutánea seca y escamosa que suele presentarse en diversas zonas del cuerpo y también puede aparecer en el glande. Cuando la psoriasis afecta el glande, se suele tratar con un **esteroide de potencia suave o media, un compuesto tópico suave de alquitrán de hulla, crema de calcipotrieno** (un tipo de vitamina D que actúa ralentizando el crecimiento celular de la piel) o un **inhibidor tópico de la calcineurina (crema de pimecrolimus o ungüento de tacrolimus)**. [49] [50] [51] [52]
- La **neoplasia intraepitelial peneana** es el nuevo término que describe todas las **lesiones dermatológicas precancerosas** del pene, reemplazando términos anteriores como enfermedad de Bowen, papulosis bowenoide, carcinoma escamoso in situ del pene y eritroplasia de Queyrat. Estas afecciones ahora se clasifican como cánceres de pene premalignos o malignos tempranos. El diagnóstico y la diferenciación se basan en histopatología, inmunohistoquímica, dermatoscopia y microscopía confocal de reflectancia. [53] La neoplasia intraepitelial peneana suele asociarse con balanopostitis, fimosis, liquen plano, liquen escleroso, fármacos inmunosupresores, trasplante de órganos, VPH y verrugas genitales. [54]. El tratamiento es variado e individualizado, pero puede incluir terapias tópicas, como **imiquimod y fluorouracilo**; **terapia fotodinámica** con metil aminolevulinato tópico seguido de exposición a luz roja de banda estrecha; **radioterapia; ablación láser; escisión quirúrgica; cirugía micrográfica de Mohs; curetaje con cauterización; y crioterapia**. [53]
La balanitis y la balanopostitis suelen tener buen pronóstico con el tratamiento adecuado. Implementar **medidas de higiene óptimas**, especialmente en hombres mayores no circuncidados con diabetes, puede reducir significativamente la incidencia de estas afecciones.
Reconocer tempranamente que un **fracaso del tratamiento** podría ser un indicio temprano de **carcinoma de pene** es crucial para minimizar la morbilidad y la mortalidad asociadas con estos cánceres.
Las **complicaciones** asociadas con la balanitis incluyen **dolor, lesiones ulcerativas del glande o prepucio, fimosis, parafimosis, estenosis meatal o uretral y la transformación maligna de lesiones premalignas**.
Referencias
- Edwards S. Balanitis y balanopostitis: una revisión. Genitourin Med. Junio de 1996; 72 (3):155-9. [ Artículo gratuito de PMC ] [ PubMed ]
- Vohra S, Badlani G. Balanitis y balanopostitis. Urol Clin North Am. Febrero de 1992; 19 (1):143-7. [ PubMed ]
- Nyirjesy P, Sobel JD. Infecciones micóticas genitales en pacientes con diabetes. Postgrad Med. Mayo de 2013; 125 (3):33-46. [ PubMed ]
- Lisboa C, Ferreira A, Resende C, Rodrigues AG. Balanopostitis infecciosa: manejo, características clínicas y de laboratorio. Int J Dermatol. febrero de 2009; 48 (2):121-4. [ PubMed ]
- David LM, Walzman M, Rajamanoharan S. Colonización genital e infección por cándida en varones heterosexuales y homosexuales. Genitourin Med. 1997 Oct; 73 (5):394-6. [ Artículo gratuito de PMC ] [ PubMed ]
- Mayser P. Infecciones micóticas del pene. Andrología. 1999; 31 Supl. 1 :13-6. [ PubMed ]
- Kalra S, Chawla A. Diabetes y balanopostitis. J Pak Med Assoc. Agosto de 2016; 66 (8):1039-41. [ PubMed ]
- Morris BJ, Krieger JN, Klausner JD. Las recomendaciones de los CDC sobre la circuncisión masculina representan una medida clave de salud pública. Glob Health Sci Pract. 24 de marzo de 2017; 5 (1):15-27. [ Artículo gratuito de PMC ] [PubMed ]
- Pow-Sang MR, Ferreira U, Pow-Sang JM, Nardi AC, Destefano V. Epidemiología e historia natural del cáncer de pene. Urología. Agosto de 2010; 76 (2 Supl. 1):S2-6. [ PubMed ]
- Douglawi A, Masterson TA. Actualizaciones sobre la epidemiología y los factores de riesgo del cáncer de pene. Transl Androl Urol. Octubre de 2017; 6 (5):785-790. [ Artículo gratuito de PMC ] [ PubMed ]
- Letendre J, Saad F, Lattouf JB. Cáncer de pene: ¿Qué novedades hay? Curr Opin Support Palliat Care. Septiembre de 2011; 5 (3):185-91. [ PubMed ]
- Morris BJ, Gray RH, Castellsague X, Bosch FX, Halperin DT, Waskett JH, Hankins CA. El fuerte efecto protector de la circuncisión contra el cáncer de pene. Adv Urol. 2011; 2011 :812368. [ Artículo gratuito de PMC ] [ PubMed ]
- Minhas S, Manseck A, Watya S, Hegarty PK. Cáncer de pene: prevención y afecciones premalignas. Urología. Agosto de 2010; 76 (2 Supl. 1):S24-35. [ PubMed ]
- Tom WW, Munda R, First MR, Alexander JW. Autodigestión del glande y la uretra mediante enzimas exocrinas pancreáticas trasplantadas activadas. Cirugía. Julio de 1987; 102 (1):99-101. [ PubMed ]
- Borelli S, Lautenschlager S. [Diagnóstico diferencial y tratamiento de la balanitis]. Hautarzt. enero de 2015; 66 (1):6-11. [ PubMed ]
- Lam K, Cook DK. Balanitis crónica: ¿Cuándo debemos preocuparnos? Aust J Gen Pract. Diciembre de 2020; 49 (12):839-841. [ PubMed ]
- Morris BJ, Krieger JN. Trastornos inflamatorios de la piel del pene y el papel preventivo de la circuncisión. Int J Prev Med. 2017; 8:32 . [ Artículo gratuito de PMC ] [ PubMed ]
- Fakjian N, Hunter S, Cole GW, Miller J. Un argumento a favor de la circuncisión. Prevención de la balanitis en adultos. Arch Dermatol. Agosto de 1990; 126 (8):1046-7. [ PubMed ]
- Schoen EJ. Circuncisión neonatal y cáncer de pene. La evidencia de que la circuncisión es protectora es abrumadora. BMJ. 6 de julio de 1996; 313 (7048):46; respuesta del autor 47. [ Artículo gratuito de PMC ] [ PubMed ]
- Talapko J, Meštrović T, Škrlec I. Creciente importancia de la candidiasis urogenital en personas con diabetes: Una revisión narrativa. World J Diabetes. 15 de octubre de 2022; 13 (10):809-821. [ Artículo gratuito de PMC ] [ PubMed ]
- Van Howe RS, Hodges FM. La carcinogenicidad del esmegma: desmintiendo un mito. J Eur Acad Dermatol Venereol. Octubre de 2006; 20 (9):1046-54. [ PubMed ]
- Johnsson KM, Ptaszynska A, Schmitz B, Sugg J, Parikh SJ, List JF. Vulvovaginitis y balanitis en pacientes con diabetes tratadas con dapagliflozina. J Diabetes Complications. 2013 sep-oct; 27 (5):479-84. [ PubMed ]
- Njomnang Soh P, Vidal F, Huyghe E, Gourdy P, Halimi JM, Bouhanick B. Infecciones urinarias y genitales en pacientes con diabetes: Cómo diagnosticarlas y cómo tratarlas. Diabetes Metab. Febrero de 2016; 42 (1):16-24. [ PubMed ]
- Arakaki RF. Inhibidores del cotransportador sodio-glucosa tipo 2 e infecciones del tracto genital y urinario en la diabetes tipo 2. Postgrad Med. Mayo de 2016; 128 (4):409-17. [ PubMed ]
- Dave CV, Schneeweiss S, Patorno E. Riesgo comparativo de infecciones genitales asociadas con inhibidores del cotransportador de sodio-glucosa tipo 2. Diabetes Obes Metab. Febrero de 2019; 21 (2):434-438. [ Artículo gratuito de PMC ] [ PubMed ]
- Kumar S, Mahajan BB, Ahluwalia RS, Boparai AS. Enfermedad de Reiter: Balanitis circinada como única manifestación previa – Tratamiento exitoso con crema de pimecrolimus al 1%. Indian J Sex Transm Dis AIDS. Enero-junio de 2015; 36 (1):70-3. [ Artículo gratuito de PMC ] [ PubMed ]
- Edwards SK, Bunker CB, Ziller F, van der Meijden WI. Guía europea de 2013 para el tratamiento de la balanopostitis. Int J ETS SIDA. Agosto de 2014; 25 (9):615-26. [ PubMed ]
- Panigrahi A, Biswas SK, Sil A. Dermatoscopia de balanitis circinada. Indian Dermatol Online J. 2021 mayo-junio; 12 (3):488-489. [ Artículo gratuito de PMC ] [ PubMed ]
- Birley HD, Walker MM, Luzzi GA, Bell R, Taylor-Robinson D, Byrne M, Renton AM. Características clínicas y tratamiento de la balanitis recurrente; asociación con atopia y lavado genital. Genitourin Med. Oct. 1993; 69 (5):400-3. [ Artículo gratuito de PMC ] [ PubMed ]
- Edwards SK, Bunker CB, van der Snoek EM, van der Meijden WI. Guía europea de 2022 para el tratamiento de la balanopostitis. J Eur Acad Dermatol Venereol. junio de 2023; 37 (6): 1104-1117. [ PubMed ]
- Randjelovic G, Otasevic S, Mladenovic-Antic S, Mladenovic V, Radovanovic-Velickovic R, Randjelovic M, Bogdanovic D. Streptococcus pyogenes como causa de vulvovaginitis y balanitis en niños. Pediatr Int. Abr. 2017; 59 (4):432-437. [ PubMed ]
- Marques TC, Sampaio FJ, Favorito LA. Tratamiento de la fimosis con esteroides tópicos y anatomía del prepucio. Int Braz J Urol. 2005 jul-ago; 31 (4):370-4; discusión 374. [ PubMed ]
- Ashfield JE, Nickel KR, Siemens DR, MacNeily AE, Nickel JC. Tratamiento de la fimosis con esteroides tópicos en 194 niños. J Urol. Marzo de 2003; 169 (3):1106-8. [ PubMed ]
- Moreno G, Ramirez C, Corbalán J, Peñaloza B, Morel Marambio M, Pantoja T. Corticosteroides tópicos para el tratamiento de la fimosis en niños. Cochrane Database Syst Rev. 2024, 25 de enero; 1 (1):CD008973. [ Artículo gratuito de PMC ] [ PubMed ]
- Ludvigson AE, Beaule LT. Urgencias Urológicas. Surg Clin North Am. Junio de 2016; 96 (3):407-24. [ PubMed ]
- Pulido-Perez A, Suarez-Fernandez R. Balanitis circinada. N Inglés J Med. 12 de enero de 2017; 376 (2): 157. [ PubMed ]
- Salloum A, Bazzi N, Saad W, Bachour J, Mégarbané H. Balanitis queratósica y micácea pseudoepiteliomatosa: Una revisión de la literatura. Australas J Dermatol. Agosto de 2021; 62 (3):421-426. [ PubMed ]
- Hanumaiah B, Mohan, Lingaiah NB, Kumaraswamy SK, Vijaya B. Balanitis queratósica y micácea pseudoepiteliomatosa: una afección poco común tratada con éxito con 5-fluorouracilo tópico. Indian J Dermatol. Noviembre de 2013; 58 (6):492. [ Artículo gratuito de PMC ] [ PubMed ]
- Wu M, Fischer G. Psoriasis genital en adultos: Una revisión actualizada para médicos. Australas J Dermatol. Mayo de 2024; 65 (3):e1-e12. [ PubMed ]
- Hong JJ, Mosca ML, Hadeler EK, Brownstone ND, Bhutani T, Liao WJ. Psoriasis genital e inversa/intertriginosa: Una revisión actualizada de terapias y recomendaciones para el manejo práctico. Dermatol Ther (Heidelb). Junio de 2021; 11 (3):833-844. [ Artículo gratuito de PMC ] [ PubMed ]
- Kelly A, Ryan C. Psoriasis genital: Impacto en la calidad de vida y opciones de tratamiento. Am J Clin Dermatol. Octubre de 2019; 20 (5):639-646. [ PubMed ]
- Beck KM, Yang EJ, Sanchez IM, Liao W. Tratamiento de la psoriasis genital: Una revisión sistemática. Dermatol Ther (Heidelb). Diciembre de 2018; 8 (4):509-525. [ Artículo gratuito de PMC ] [ PubMed ]
- Palaniappan V, Karthikeyan K. Enfermedad de Bowen. Indian Dermatol Online J. 2022 mar-abr; 13 (2):177-189. [ Artículo gratuito de PMC ] [ PubMed ]
- Kristiansen S, Svensson Å, Drevin L, Forslund O, Torbrand C, Bjartling C. Factores de riesgo de neoplasia intraepitelial del pene: un estudio de registro poblacional en Suecia, 2000-2012. Acta Derm Venereol. 01 de marzo de 2019; 99 (3): 315-320. [ PubMed ]

